2023.02.09-2023.03.07,国内ADC药物的新药上市/临床试验申请的受理和批准/许可信息如下:
新药上市申请(NDA)受理:无。
新药上市申请(NDA)批准:1个ADC药物(注射用德曲妥珠单抗,注射用Trastuzumab Deruxtecan)上市申请获批,为第一三共的2.2类申请。注射用德曲妥珠单抗(商品名:优赫得)是截至目前中国获批的第7个ADC药物。
新药临床试验申请(IND)受理:共4个国产ADC药物临床试验申请受理(3个首次受理;1个非首次受理,见表蓝字)。
新药临床试验申请(IND)默示许可:共2个国产ADC药物临床试验申请获默示许可(首次受理、许可)。
1、ADC药物的NDA受理/批准信息汇总
ADC药物的NDA受理信息汇总
无。
ADC药物的NDA获批信息汇总

2、ADC药物的IND受理/许可信息汇总
ADC药物的IND受理信息汇总
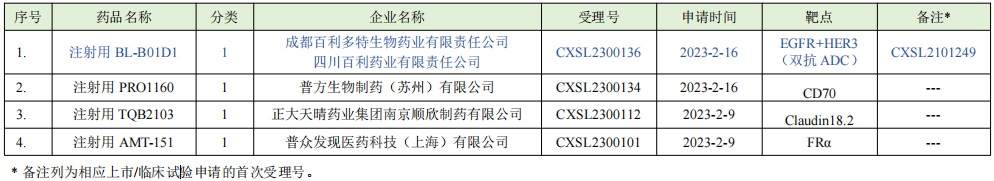
ADC药物的IND默示许可信息汇总
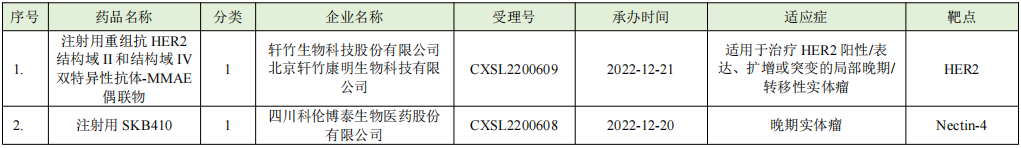
信息来源:
[1] 国家药品监督管理局药品审评中心
https://www.cde.org.cn/
[2] 国家药品监督管理局政务服务门户
https://www.nmpa.gov.cn/zwfw/index.html



