阅读量:0
2023年,ADC(抗体偶联药物)全球销售已破百亿美元,以狂暴的规模增速宣告了其为名副其实最具投资价值的创新药主流赛道之一。
中国作为全球ADC管线研发的领导者,机会黄金遍地。
3月28日,国内领先的ADC Biotech乐普生物发布2023年业绩报告:公司实现收入2.25亿元,同比增长1347.2%;年度亏损0.22亿元,相比2022年亏损6.89亿元的幅度大幅减少(缩减幅度96.8%),经调整年内净亏损减少至2.5亿元。
众所周知,在国内投融资寒冬的背景下,亏损的收窄减缓现金消耗是未盈利Biotech公司的生命线之一。
乐普生物2023年亏损大幅收窄,是通过多元化的收入结构实现的,具备十足的含金量:1)公司PD-1普特利单抗爬坡放量迅速,上市首个完整年度收入1.01亿元(2022年11月上市);2)其次,2023年内公司与康诺亚合作CLDN18.2 ADC管线CMG901完成了一项对外授权,BD及技术服务费收入1.24亿元,而随着AZ推进大三期,未来有望收到后续里程碑。另外,公司通过减持皓阳生物股权实现投资收益约1.04亿元、以及所持长期股权投资武汉滨会因股权被动稀释录得收益约1.16亿元,补充现金流的同时净亏损大幅收窄;3)公司降本增效成果显著,在研发费用方面采取资源聚焦战略,创新药价值高效转化,费用从2022年5.24亿缩减为2023年4.58亿;行政开支从2022年的1.38亿大幅缩减为0.87亿,销售及营销开支仅约为0.43亿元。
潜龙在渊,尽管乐普生物的市场关注度不如全球市场头部的几家ADC Biotech,但投资者需意识到:属于乐普生物高光时刻,很快就会到来。
瞄准未满足临床需求和最难癌种
2024年以来,针对创新药的鼓励政策全面而密集。
监管机构不仅在2024政府工作报告中首次提到“创新药”,2024年3月国务院公布了《产业结构调整指导目录(2024年本)》,目录中指出:拥有自主知识产权的创新药及抗体偶联这类的医药核心技术突破均在鼓励项之列。同月,市场广泛传播的“全链条支持创新药”政策中,也明确鼓励聚焦原始创新药物,重点支持新靶点、新机制、新结构、新技术且有自主知识产权的药物。
另一个角度而言,国家层面对国内未被满足临床需求愈发重视,最直接体现在对罕见病用药的支持上,如2023年新增126种药品中就包括15款罕见病药物,数量创近三年新高。
无论政策鼓励的方向有多广,具备足够确定性的是:只有真正具备重大创新性的药物研发厂商,才能够充分受益政策的红利。
在响应或受益创新药鼓励政策层面,乐普生物在众多国内Biotech公司中出类拔萃,其核心ADC管线从一开始就瞄准了国内未满足临床需求鼻咽癌、全球“癌王”胰腺癌。
MRG003的鼻咽癌适应症2022年获得美国孤儿药认定及中国突破性疗法认定,2023年获得美国FDA快速通道资格;MRG004A在2023年12月获得FDA的孤儿药认定,2024年初用于治疗胰腺癌获的美国FDA快速通道资格。
据2020全球癌症数据统计,全球鼻咽癌新发病例为13.3万例,其中我国新发6.24万例,占到每年新发病患数的46.92%。
尽管鼻咽癌并不算一个大癌种,但其具备发病地区集中(全球近一半在中国、国内绝大部分病例在南方地区)、早期患者接受根治性手术后&局部晚期接受放化疗患者生存期普遍较长(5年生存率分别高于95%、75%)等特点。
在鼻咽癌整体患者生存期较长的背景下,仍约有20%的晚期患者由于发生复发或远处转移而导致预后较差,现有治疗手段为姑息性化疗或免疫治疗。据2021版CSCO鼻咽癌诊疗指南,对于复发转移性鼻咽癌二线及以上治疗,推荐单药化疗或PD-1/PDL-1抑制剂治疗,客观缓解率仅20~30%,效果非常有限,急需新型药物填补临床治疗空白。
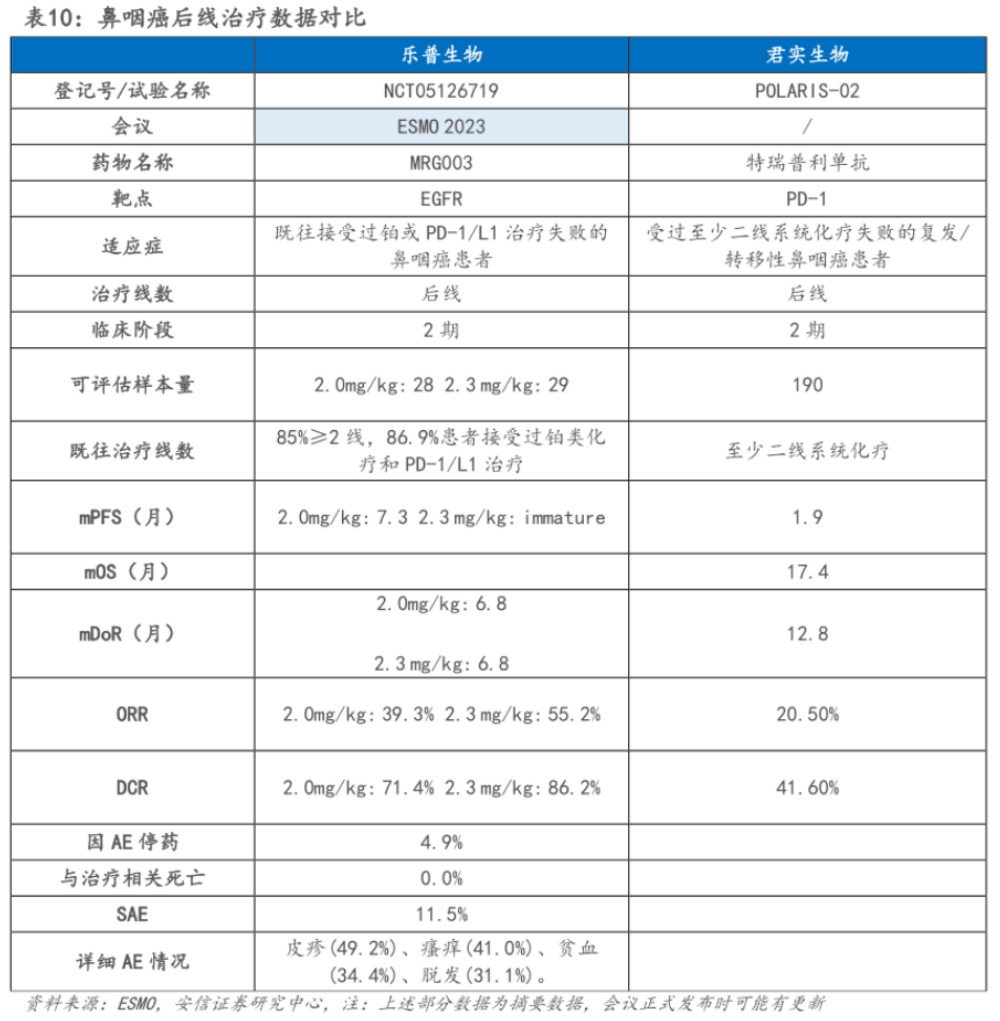
乐普生物瞄准了复发转移性鼻咽癌后线未满足治疗需求,MRG003是一款新型的EGFR ADC,而EGFR在鼻咽癌中表达率非常高(50%过表达),高表达与肿瘤侵袭性、转移和放疗/化疗抵抗增加有关,MRG003针对经铂类化疗或PD-(L)1治疗失败的鼻咽癌患者治疗的二期数据显示:其治疗组的mPFS高达7.3个月,且因AE停药患者比例仅有4.9%,无因治疗死亡事件;这意味着MRG003大概率可取得较PD-1们数倍以上的销售峰值(独家定价不内卷、用药时间长、多适应症并进),同时未来还有望进军鼻咽癌的前线治疗,预估销售峰值在15-20亿元。
图片来源:瞪羚社
胰腺癌又被称为“癌中之王”,由于胰腺癌起病隐匿、早期没有明显症状,而且诊断困难(早期发现率仅5%-7%,在所有癌症中最低),80%患者发现时已达局部晚期或者发生转移,失去了最佳手术机会。加上针对晚期患者治疗手段有限(目前以化疗为主),缺乏有效的靶向或免疫疗法,患者的总生存期仅6-9个月,致死率极高。
根据世界卫生组织发布的全球癌症负担数据显示,2020年全球约有46.6万死亡病例,中国胰腺癌新发病例和死亡病例均超过12万例。
治疗药物方面,以广谱性著称的PD-(L)1免疫疗法,对胰腺癌依旧束手无策,大部分临床都遭遇失败;即便是ADC中的药王选手DS-8201在面对HER2表达晚期胰腺癌时也束手无策,已有的二期数据确认ORR仅有4%,是所有适应症中疗效最差的。在NCCN指南也指出,一线治疗晚期胰腺癌mOS一般在10个月以内,接受二线治疗后mOS更是只有约6个月。
不过,全球在研管线中只有极少数在研管线被认为具备治疗胰腺癌的潜力,TF ADC便是其中一类药物。目前,全球范围内Seagen/Genmab的TF ADC产品Tivdak获批上市,由于其在宫颈癌、卵巢癌、头颈癌等亦有潜力,机构预测其销售峰值可能超过12亿美金。
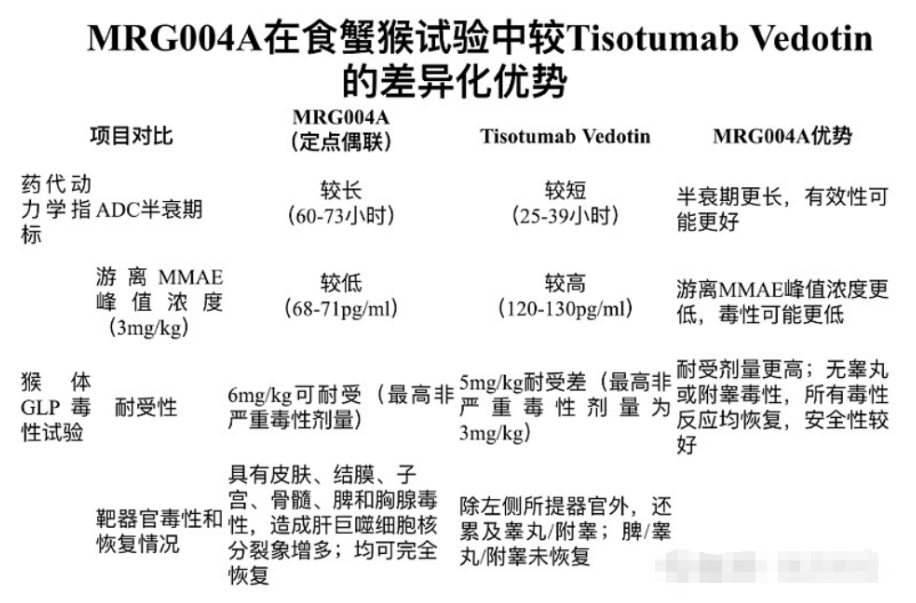
乐普生物也是TF ADC赛道的领导者,其管线MRG004A正在中美进行一期临床,相比于已上市的Tivdak,MRG004A具备更长的半衰期、更好的耐受性,对应更宽的治疗窗,有望成为TF ADC赛道的同类最佳。
图片来源:瞪羚社
商业化与BD双重预期
一分耕耘,一分收获。
乐普生物持续押注市场核心赛道、攻克未满足临床需求,正向反馈将接踵而至,不仅公司现有ADC管线具备很强的授权潜力,同时部分ADC管线产品也进入商业化倒计时。

图片来源:瞪羚社
MRG003是全球为数不多进入三期的EGFR ADC,也是国内在研进度最快EGFR ADC。
EGFR这个靶点相信国内投资者耳熟能详,在小分子领域其诞生了众多替尼类重磅炸弹,随着EGFR-TKI耐药患者越来越多,靶向EGFR的ADC药物便成为了巨头们眼中的“香饽饽”。
MNC中,艾伯维重金从外部引进了数个EGFR ADC,却屡屡以临床数据不及预期而折戟;另一边,AZ在与科伦博泰、第一三共合作后,也正在积极的扩展不同靶点的ADC版图,大热的EGFR ADC极有可能成为目标。
乐普生物的MRG003不仅在全球进度领先,成药性已经让市场吃下了一颗“定心丸”。MRG003在PD-1及化疗经治的鼻咽癌患者IIa临床数据显示:2mg/kg的低剂量组ORR为39.3%,mPFS为7.3个月;2.3mg/kg的中高剂量组ORR为55.2%,mPFS仍不成熟。MRG003在后线鼻咽癌数据层面已展现远优于PD-1们的疗效,并且MRG003计划在2024年下半年报产。
另外,MRG003在PD-1及化疗经治的头颈癌患者二期上录得了同样优异的疗效数据(ORR与mOS分别为43%、11.3个月),目前已经进入了三期临床阶段。
MRG004A同样拥有浓烈的BD预期,组织因子TF同样是潜力很大的ADC靶点,其在乳腺癌、肺癌、结肠癌、胰腺癌等多种癌症上过表达。
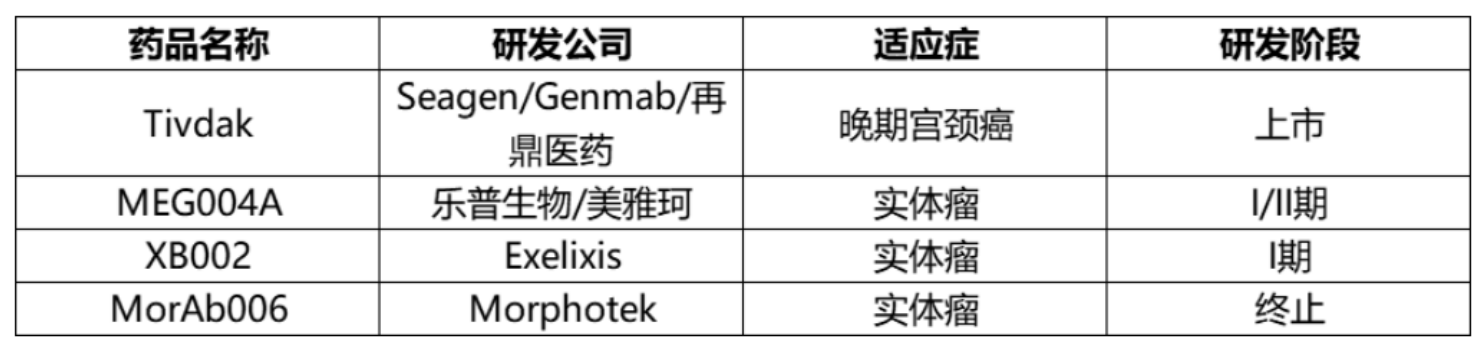
目前Seagen的Tivdak已经拿下了宫颈癌、卵巢癌两大适应症,但其较高的眼毒性和现有适应症空间构成了其当下的天花板;与Tivdak相比,乐普生物的MRG004A具备很强的差异化,不仅包括在前文提到拥有更好的耐受性、更大的治疗窗,而且公司在临床上已经观察到其胰腺癌(PC)、TNBC(三阴乳腺癌)及CC(宫颈癌)的治疗潜力。
尤其在胰腺癌领域,一旦MRG004A在早期数据中展现出初步的疗效和安全性,届时压根不愁买家。
图片来源:瞪羚社
同时,投资者不应该忽视的是,乐普生物的HER2 ADC管线MRG002离商业化也差临门一脚,目前除了针对HER2高表达乳腺癌肝转移患者正在进行二期临床外,针对HER2 高表达乳腺癌适应症正在进行临床三期。
这么看来,乐普生物不仅拥有一般Biotech没有的多款管线强烈BD预期,同时最快在2025年公司将有2-3款产品在市销售(PD-1普特利单抗、MRG003或MRG002)。那么,可以预见乐普生物有望在未来几年收入规模快速提升,达到盈亏平衡并实现盈利指日可待。
优势扩围:联合疗法
IO+ADC取代IO疗法成为未来各大实体瘤前线治疗的趋势已经无法阻挡,K药联合Nection-4 ADC(Padcev)治疗一线晚期膀胱癌已经挑战成功。同样来势汹汹的,还有IO+溶瘤病毒组合。
在下一代疗法的革命浪潮中,乐普生物在国内创新药企甚至全球药企中拥有绝对的前瞻性。
目前,乐普生物拥有了已商业化的PD-1普特利单抗,ADC也即将拥有MRG003、MRG002这样后期冲刺商业化产品,同时公司还有全球当下最稀缺的溶瘤病毒产品。对于IO、ADC和溶瘤病毒这三个领域有着全方位布局的企业,全球Biotech可能不超过3家(MNC除外)。
实质上,溶瘤病毒是个“老药”并不稀缺,但成药且蕴含磅礴治疗潜力的溶瘤病毒无比稀缺,乐普生物通过与CG Oncology合作,在很早期拿到了溶瘤病毒CG0070其大中华区的权益。
CG0070在其最新的针对高危BCG无反应非肌层浸润性膀胱癌临床三期中期分析中,CG0070治疗组患者的完全缓解率达到75.7%;用药3个月及6个月CR为68.2%及63.6%,其中74.4%患者完全缓解维持6个月以上。CG0070治疗的112例患者中,3级及以上副作用发生率为0,没有副作用导致的停药病例,没有死亡病例。
更重要的是,在CG0070联合K药针对高危BCG无反应非肌层浸润性膀胱癌早期临床数据中,91%患者接受3个月联合治疗获得缓解,到了12个月仍有75%患者维持完全缓解。这意味着,两者联合用药患者完全缓解率数据较单药有着数倍以上的提升。这也是在这个适应症中目前看到的最好的一个治疗方案。
CG Oncology的CG0070三期临床已进入尾声,目前,乐普生物CG0070正在进行国内的一期临床。对于公司而言,只需要在CG0070海外获批之前完成一期临床,由于有大量海外临床的确证性数据,做完一期临床后大概率可跟监管机构沟通直接开展小规模桥接三期临床,实现快速上市。
IO、ADC和溶瘤病毒单品均处于商业化阶段后,其疗效和安全性经过充分验证,此时及后续公司想要布局绝大多数适应症的联用,可能相比其他大部分同行,在入组、监管沟通、审批等流程上将拥有更高的效率和优势。
当然除了这个小算盘之外,在探索IO+ADC、IO+溶瘤病毒联合疗法方面,乐普生物也走在了国内创新药企业的最前头。
目前,乐普生物正在进行两个方向的二期临床,分别是普特利单抗+MRG003探索鼻咽癌及头颈癌的治疗应用、普特利单抗+MRG002治疗HER2表达实体瘤的治疗应用。另外,普特利单抗与CG0070联合治疗高危BCG无反应非肌层浸润性膀胱癌的I/II临床也正计划开展。
早期临床多瘤种潜力的初步探索和验证,其实也是为了乐普生物未来开展联合疗法大三期进行探路,也方便配合后续公司各个单药上市后能够迅速开展各个适应症的注册性临床,确保公司走在国内的最前沿。
结语:乐普生物正在积极的通过不同手段快速抵御医药投融资寒冬带来的负反馈,这是一家优秀的Biotech所应该具备的行动策略和特质。但除了这些之外,我们更多的能看到公司所蕴含的潜力和商业化机会,价值修复可能仅仅需要时间的洗礼。
对于乐普生物这样的“小而美”ADC Biotech选手,我想弹性之外,更多的或许是确定性。



